廣效性流感疫苗研發突破
流感病毒知多少?
流感是由病毒引發的傳染病,幾乎每個人都得過流感,但你親眼看過這些磨人的小東西嗎?(喂!)
流感病毒直徑約 80~120 奈米,入侵細胞全靠外套膜上兩種醣蛋白:一種是血凝集素(Hemagglutinin,簡稱 HA),能幫助病毒黏附宿主細胞,一種是神經胺酸酶 (Neuraminidase,簡稱 NA),幫助病毒在宿主細胞內繁殖後離開、持續在宿主體內擴散。
採訪編輯: 歐宇甜、黃曉君
美術編輯: 林洵安
流感是由病毒引發的傳染病,幾乎每個人都得過流感,但你親眼看過這些磨人的小東西嗎?(喂!)
流感病毒直徑約 80~120 奈米,入侵細胞全靠外套膜上兩種醣蛋白:一種是血凝集素(Hemagglutinin,簡稱 HA),能幫助病毒黏附宿主細胞,一種是神經胺酸酶 (Neuraminidase,簡稱 NA),幫助病毒在宿主細胞內繁殖後離開、持續在宿主體內擴散。
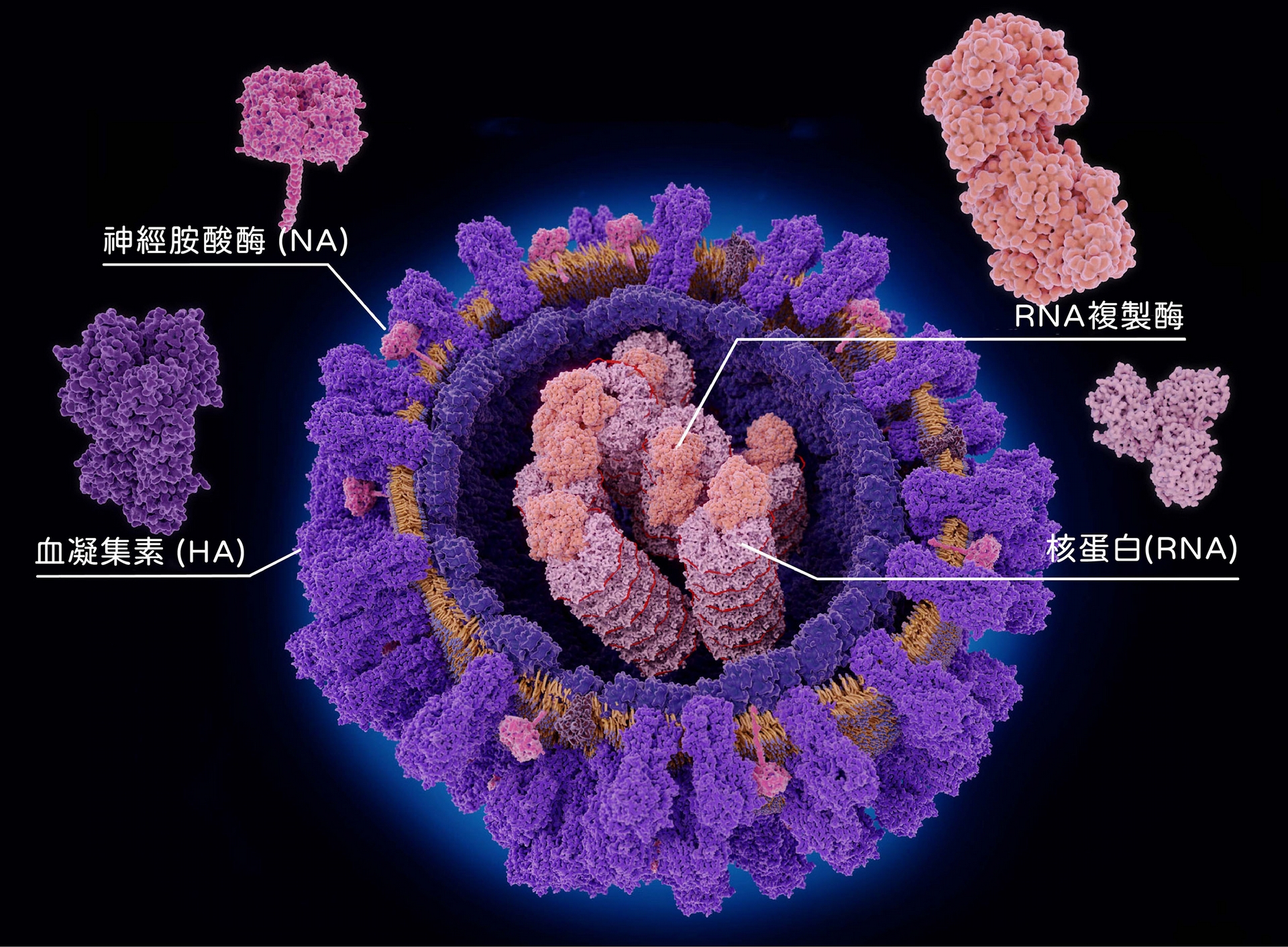
流感病毒直徑約 80~120 奈米,因為是 RNA 病毒,非常容易變異。入侵細胞全靠外套膜上兩種醣蛋白:一種是血凝集素(Hemagglutinin,簡稱 HA),能幫助病毒黏附宿主細胞,一種是神經胺酸酶 (Neuraminidase,簡稱 NA),幫助病毒在宿主細胞內繁殖後離開、持續在宿主體內擴散。 圖│iStock
會感染人類的流感病毒又可分為 A、B、C 三型:
A 型病毒的 HA 共 18 種 (H1 ~ H18),NA 共 9 種 (N1 ~ N9),不同的 HA 和 NA 可組成不同亞型 (subtype),如 H1N1 表示有 HA1 和 NA1 兩種蛋白質,常感染人類的有 H1N1、H3N2 三種。
A 型流感病毒的變異很快,而且可能在人群中迅速傳播而造成嚴重疫情,像 1918 年西班牙 H1N1 流感曾大流行,導致全球至少2000萬人死亡,宛如中世紀的黑死病!
B 型病毒沒有亞型,也不會快速變異,雖會導致大流行,不會導致嚴重疫情。C 型也沒有亞型,感染後只出現輕微症狀,不會導致大流行。
人類在 1944 年,發明了第一個 A 型流感疫苗,終於有了武器控制流感大流行,但這場人與病毒的戰爭並未真的完結!因為流感疫苗,可是唯一需要年年改換病毒株的人用疫苗。
流感病毒在全球傳播後,在不同的地區可能變異成新的病毒株 (strain),如 B 型流感有維多利亞株、山形株,A 型流感有 H1N1 加州株、H3N2 維多利亞株等,導致舊的疫苗失效。
為了對抗不斷變化的流感病毒,世界衛生組織 (WHO) 在各國設有偵測中心,從各處的病患和鳥類身上採樣、蒐集流感病毒資訊,然後每年召開北、南半球的季節性流感疫苗選株會議,預測明年可能流行的兩種 A 型病毒株、兩種 B 型病毒株,通常於來年2月公布北半球的選株結果,以利製作當年流感疫苗,臺灣地區則通常於10月開打。
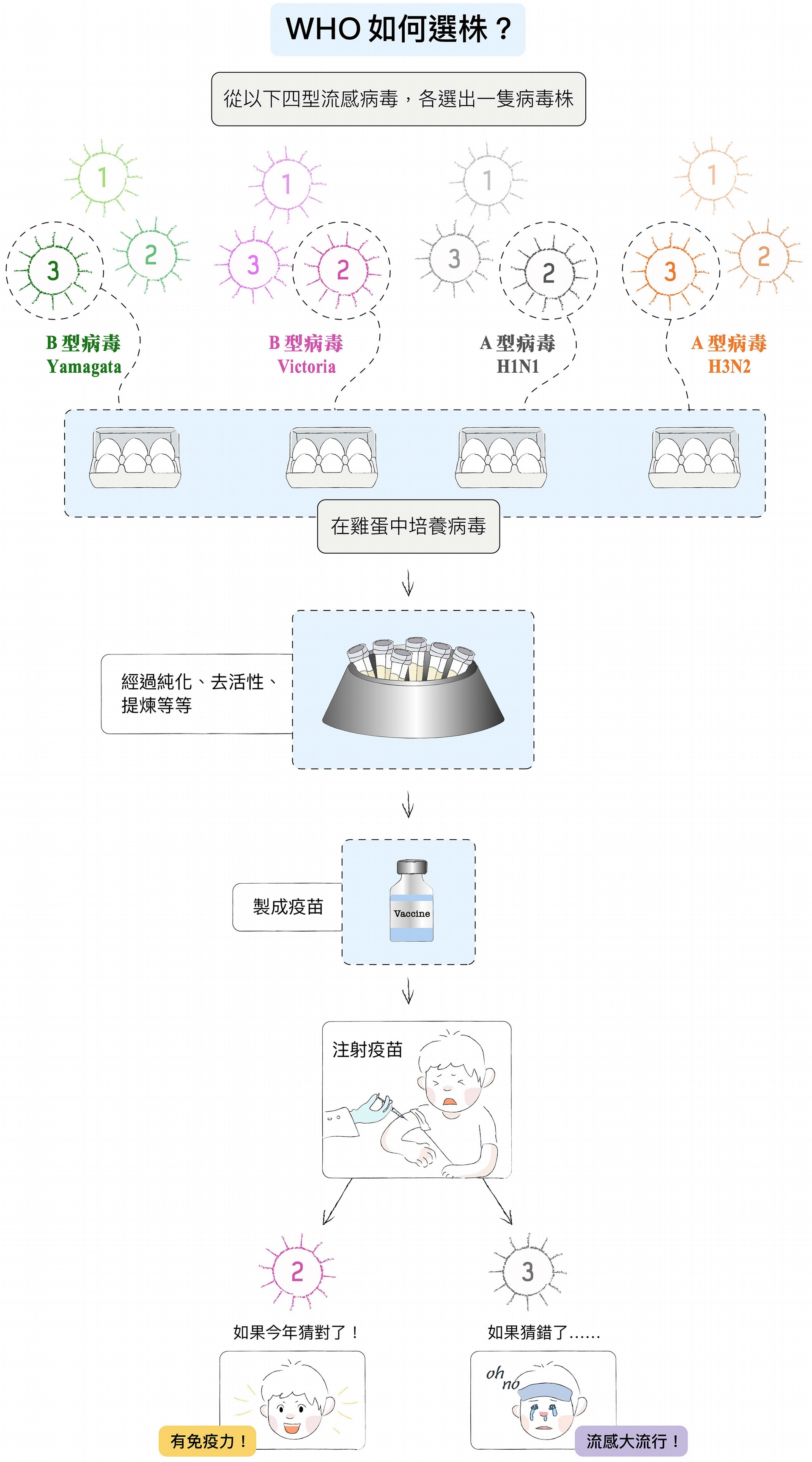
WHO 每年會從 B 型流感病毒、A 型流感病毒第一群、第二群的病毒株中,分別選出可能流行的病毒株,將它們放進雞蛋中培養,再經過純化、去活性、提煉等等步驟,製作成流感疫苗。如果猜對了,人們只要打過疫苗,就能不致染病或減輕病情,但如果猜錯了,疫苗保護力大減,恐將引發大流行。圖│研之有物 (資料來源│馬徹)
如果猜對了,打疫苗約有 70% 保護力。但預測常趕不上病毒的變化!一旦猜錯,只剩 20~30% 保護力,恐導致全球大流行。因此全球科學家一直希望找出廣效性流感疫苗,可以對抗流感所有的病毒株。
這件事異常困難,因為病毒的 HA 和 NA 太常發生突變,同一亞型、不同株的變異程度只要有 5% 到 20%,即可能讓疫苗保護力失效。如何解決病毒一直變異、疫苗無法有效保護的問題?翁啟惠與馬徹的研究團隊發現,可從破解 HA 的構造開始。
仔細觀察,HA 的外型像蘑菇,分為膨大的「頂部」和固定在外套膜上的較細「莖部」,通常免疫系統只能辨識 HA 頂部,目前的流感疫苗多半也是利用 HA 頂部作為抗原、誘發免疫系統生產抗體。但 HA 頂部非常容易發生突變,所以選株才會這麼困難。馬徹團隊則另闢蹊徑,從 HA 不容易變異的莖部下手!
原來流感病毒很狡猾,會奴役宿主細胞幫忙做出一顆顆醣,黏在自己的 HA 上,通常莖部的醣分子比頂部更多。病毒利用這些醣分子當成偽裝,好像在臉上戴上醣面具,讓免疫系統誤以為病毒是「自己人」。
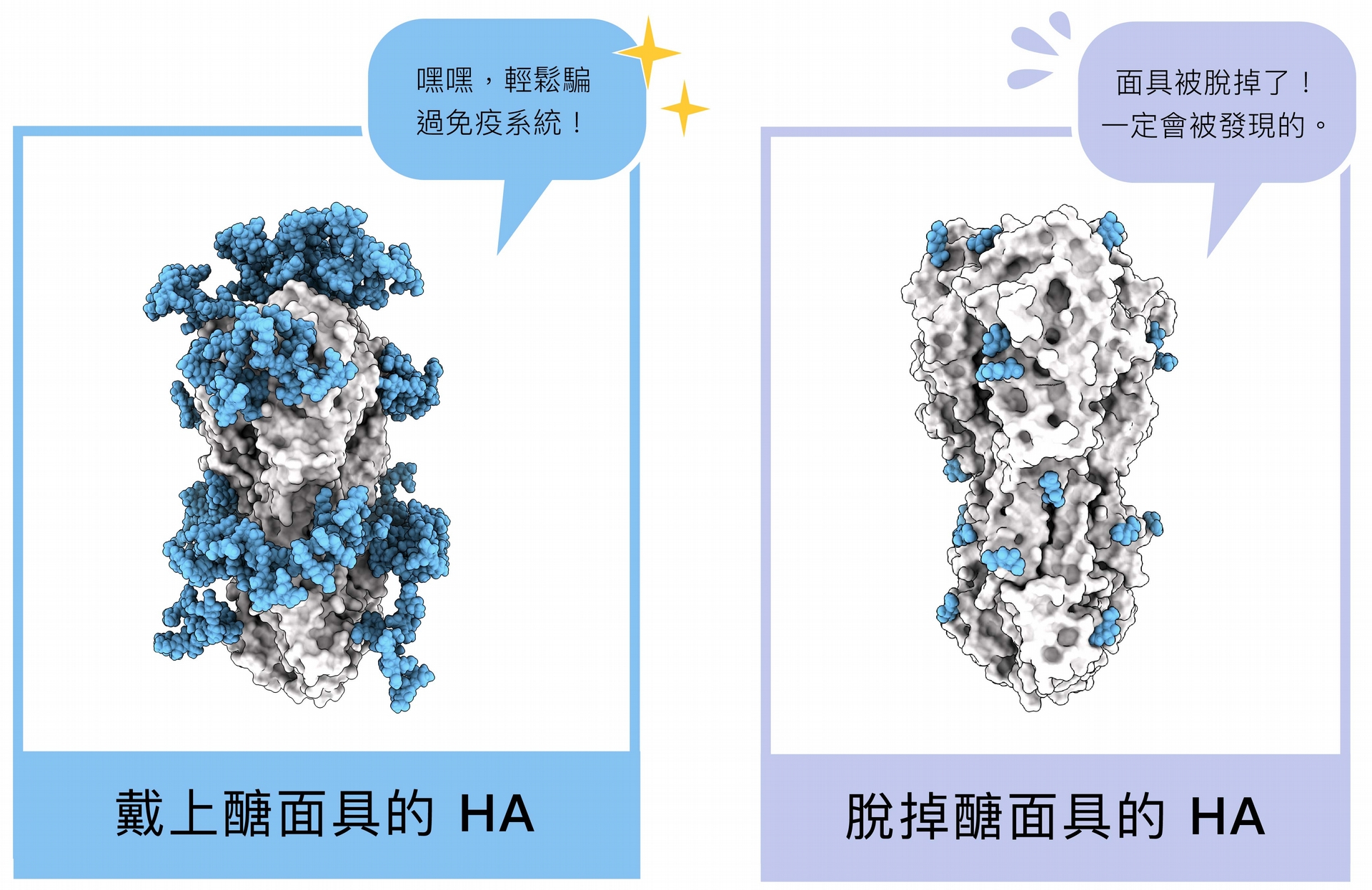
HA 醣蛋白結構,藍色部分即為醣面具,左圖為原本布滿醣分子的結構,右圖為研究員拿掉絕大多數醣分子後、還原 HA 的真面目。 圖│研之有物 (資料來源│馬徹實驗室)
「病毒在傳播時, HA 莖部有許多醣蓋住,形成一種保護,不易被宿主偵測,因此這些部位變異的壓力小,胺基酸序列的變異也比較小。」馬徹點出關鍵:「換句話說,不同病毒株的 HA 莖部變異應該不大。」
馬徹團隊進一步發現,如果將流感病毒 HA 莖部附近的醣拿掉、將這部分片段製成疫苗,如同揭去病毒的「面具」(醣),讓宿主的免疫系統辨識病毒的「臉」(HA 的莖部 )。
"這麼一來,即使病毒換幾頂新款式的帽子 (HA 的頂部變異) 也無妨,免疫系統依然能認出病毒的臉 (HA 的莖部)。"
他與研究團隊隨即展開新型流感疫苗的研發,選擇一般流感疫苗的製程——以雞蛋培養病毒,只在其中修改了兩個步驟:在雞蛋裡加入抑制劑,打斷病毒製醣過程、做到一半就停止,再加入像剪刀的酵素,剪去多餘的醣,使 HA 只剩一顆單醣。經過不斷嘗試,終於成功研發出單醣化的流感疫苗。
細心的讀者可能會發現:既然要除去病毒的偽裝,為何不乾脆把全部的醣分子去掉,仍然留下一顆「單醣」呢?翁啟惠院士在醣分子研究曾發現,細胞不是做完蛋白質才開始裝醣分子,而是一邊做、一邊裝,第一顆醣分子對醣蛋白的摺疊過程很重要,能決定醣蛋白結構。馬徹也發現如果把醣全部切掉,HA 穩定度不好,所以決定讓病毒先製作醣、HA 摺疊正確,再加入抑制劑和酵素,剪去多餘的醣、只留下一顆。
他們將單醣流感疫苗打到小鼠、雪貂身上,證實誘發的免疫反應變好,不但抗莖部抗體 (anti-stem antibodies) 變多,抗體媒介細胞毒殺作用 (Antibody-dependent cellular cytotoxicity,簡稱 ADCC,指抗體能和巨噬細胞、殺手細胞結合,把被病毒感染的細胞清除)的效果也提高。
馬徹表示,「雖然只把現有疫苗做小修改,卻能獲得更大保護力。同一亞型但不同病毒株的莖部變異較小,單醣流感疫苗對於同一亞型可以通用,未來如果把流感疫苗的四價 (四種病毒株) 都開發單醣化,就不用每年改成分,只要等病毒變化很大再更新即可。 」研究成果於 2019 年 2 月獲刊於《美國國家科學院學報》。
2020 年 7 月,團隊再傳捷報!博士後研究員廖心瑜將來自兩種不同病毒株 (H5和H1) 的蛋白質,結合成一個頭部含有共通 H5 序列、莖部含有共通 H1 序列的嵌合蛋白,再輔以上述的單醣化技術,研發出「單醣化嵌合血凝集素蛋白疫苗」,可預防各種異株和亞型的 A 型流感病毒感染人體,同樣獲登《美國國家科學院學報》。 相信未來翁啟惠和馬徹團隊還有更多的好消息,逐步實現廣效性流感疫苗的夢想!
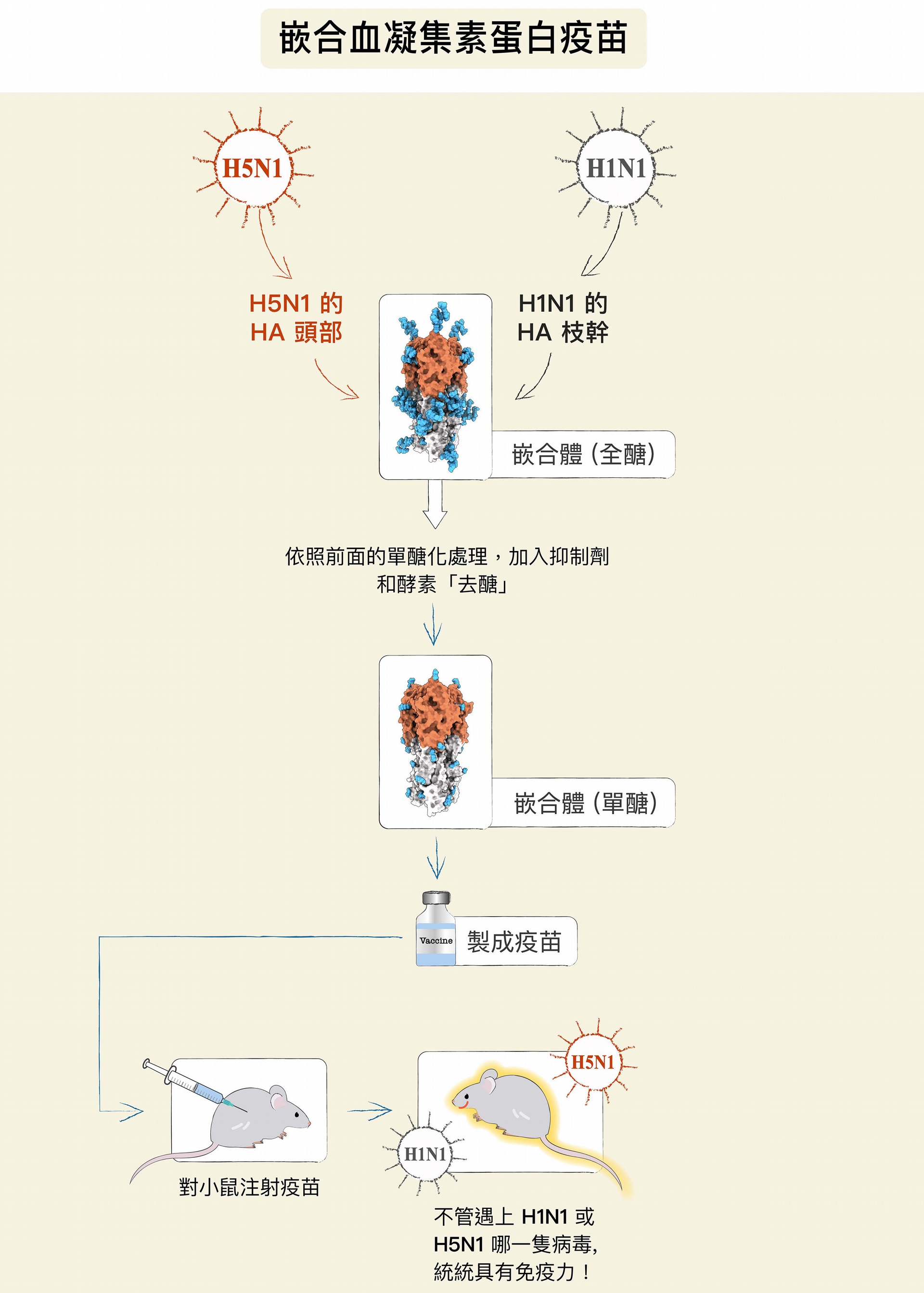
博士後研究員廖心瑜將來自兩種不同病毒株 (H5和H1) 的蛋白質,結合成一個頭部含有共通 H5 序列、枝幹含有共通 H1 序列的嵌合蛋白,再輔以上述的單醣化技術 (藍色為醣類),研發出「單醣化嵌合血凝集素蛋白疫苗」,可預防各種異株和亞型的 A 型流感病毒感染人體。 圖│研之有物 (資料來源│廖心瑜)
回首這些突破性研究的靈感來源,馬徹微笑「老實說」:「其實一開始,我壓根沒想到這個可以開發出流感疫苗。」
馬徹在博士班的研究領域為蛋白質結構學,對於流感病毒並不熟悉。2004 年他進入中研院,那時基因體研究中心剛成立,時任主任的翁啟惠召集各實驗室研究流感、抗藥性細菌感染和癌症,馬徹才開始接觸流感病毒,並負責研究蛋白質結構。
在一次偶然的發現中,他注意到 HA 這種醣蛋白很怪異:「 HA 會跟宿主的醣分子結合,但自己的表面又有一堆醣,這些醣是要做什麼用?對 HA 的功能有什麼影響嗎?」出自好奇心的驅使,他把 HA 上的醣從外面依序愈切愈短,有的切到只剩下一顆醣,觀察帶有不同數量醣分子的 HA 跟細胞結合的狀況。
結果發現,當 HA 的醣愈少,跟細胞結合力愈好。這個結果引起他更大疑惑:「既然如此,HA 幹嘛要裝上那麼多醣呢?」繼續研究後發現:HA 的醣分子能形成偽裝、躲避免疫系統攻擊。於是他嘗試在實驗室製造兩種 HA,一個帶有醣,一個不帶醣,送去生產抗體試劑,再進行簡單的測試,果然發現不帶醣的 HA 抗體反應性很高。
當馬徹在會議上報告完這項「有趣的」實驗發現,翁啟惠立刻說:「這會是一個好疫苗!」
「那次翁老師說完後,現場20、30個人包括我,根本不知道他在講什麼,全場都傻眼。」但馬徹想了一下,終於恍然大悟:病毒利用醣分子偽裝自己,如果去掉這些醣分子,應該能誘發更好的免疫反應。馬徹回憶:
"那次經歷讓我真正感受到科學家見微知著的能力 ,翁啟惠老師只看到一點點線索,就能跳躍好幾步思考。"
「中研院最重要的角色就是做基礎研究,但所有的應用起初都從基礎研究來的。有時並不是計劃或預期的發現,卻可能有很棒的應用。」馬徹總結:「我覺得當科學家很幸運、好玩,即使研究流感已十幾年,仍有許多未知等待被發現。」
正是馬徹永無止盡的好奇心、翁啟惠專業知識累積來的深刻洞見,共同催生這一場流感疫苗的大革命。

馬徹,中研院基因體研究中心研究員暨化學生物學組執行長,為翁啟惠院士領導研究團隊重要成員,致力於開發廣效性流感疫苗。 圖│研之有物
AD